

Сила усадки будь-якої довжини одиниці на поверхні рідини називається поверхневим натягом, а одиниця-N. · M-1.

Властивість зменшення поверхневого натягу розчинника називається поверхневою активністю, а речовина з цією властивістю називається поверхнево-активною речовиною.
Поверхнево-активна речовина, яка може зв'язувати молекули у водному розчині та утворювати міцели та інші асоціації та мати високу поверхневу активність, а також вплив на змочування, емульгування, піноутворення, промивання тощо, називається ПАР.
ПАР - це органічні сполуки зі спеціальною структурою та властивостями, які можуть суттєво змінити міжфазний натяг між двома фазами або поверхневим натягами рідин (як правило, води) з змочуванням, піноутворенням, емульгуванням, промиванням та іншими властивостями.
З точки зору структури, поверхнево -активні речовини мають загальну особливість, оскільки вони містять дві групи різних характерів у своїх молекулах. На одному кінці-довгий ланцюг неполярної групи, розчинний у нафті та нерозчинні у воді, також відомий як гідрофобна група або водяна релігентна група. Така група водних вод, як правило, є довгими ланцюгами вуглеводнів, іноді також для органічного фторину, кремнію, органофосфату, органотинового ланцюга тощо. На іншому кінці є водорозчинна група, гідрофільна група або нафтопроникна група. Гідрофільна група повинна бути достатньо гідрофільною, щоб забезпечити, щоб цілі ПАР були розчинними у воді та мають необхідну розчинність. Оскільки поверхнево -активні речовини містять гідрофільні та гідрофобні групи, вони можуть бути розчинними щонайменше в одній з рідких фаз. Ця гідрофільна та ліпофільна властивість ПАР називається амфіфільністю.


ПАР - це різновид амфіфільних молекул як з гідрофобними, так і з гідрофільними групами. Гідрофобні групи поверхнево-активних речовин, як правило, складаються з довголанцюгового вуглеводнів, таких як прямо ланцюгова алкіл C8 ~ C20, гіллястий ланцюг алкил C8 ~ C20 , алкілфеніл (число TOM алкілу вуглецю-8 ~ 16) і подібне. Різниця, яка невелика між гідрофобними групами, в основному полягає в структурних змінах вуглеводневих ланцюгів. А типи гідрофільних груп більше, тому властивості ПАР в основному пов'язані з гідрофільними групами на додаток до розміру та форми гідрофобних груп. Структурні зміни гідрофільних груп більші, ніж у гідрофобних груп, тому класифікація ПАР, як правило, ґрунтується на структурі гідрофільних груп. Ця класифікація ґрунтується на тому, чи є гідрофільна група іонною чи ні, і вона розділена на аніонні, катіонні, неіонні, цвіттеріонічні та інші особливі типи ПАР.

① Адсорбція ПАР у Interfac
Молекули ПАР - це амфіфільні молекули, що мають як ліпофільні, так і гідрофільні групи. Коли поверхнево -активна речовина розчиняється у воді, його гідрофільна група притягується до води і розчиняється у воді, тоді як її ліпофільна група відштовхується водою та листям води, що призводить до адсорбції молекул поверхнево -активної речовини (або іонів) на інтерфейсі двох фаз, що зменшує міжфазний натяг між двома фазами. Чим більше молекул поверхнево -активної речовини (або іонів) адсорбуються на інтерфейсі, тим більше зменшення міжфазного напруження.
② Деякі властивості мембрани адсорбції
Поверхневий тиск адсорбційної мембрани: адсорбція поверхнево-активної речовини на інтерфейсі газо-рідини для формування адсорбційної мембрани, наприклад, розміщення знімаючого плаваючого листа, плаваючого листа, що підштовхує адсорбенту на поверхні розчину, а мембрана генерує тиск на плаваючу аркуш, який називається поверхнею.
Поверхнева в'язкість: Як і поверхневий тиск, поверхнева в'язкість - це властивість, виявлена нерозчинною молекулярною мембраною. Підвішена тонким металевим дротом платиновим кільцем, так що його площина контактує з поверхнею води в резервуарі, обертайте платиновим кільцем, платиновим кільцем за допомогою в'язкості водної перешкоди, амплітуда поступово розпадається, згідно з якою можна виміряти поверхневу в'язкість. Метод: По -перше, експеримент проводиться на чисту водну поверхню для вимірювання амплітуди розпаду, а потім розпад після утворення поверхневої мембрани вимірюється, а в'язкість поверхневої мембрани походить від різниці між ними.
Поверхнева в'язкість тісно пов'язана з міцністю поверхневої мембрани, і оскільки мембрана адсорбції має поверхневий тиск і в'язкість, вона повинна мати еластичність. Чим вище поверхневий тиск і чим вище в'язкість адсорбованої мембрани, тим вище її пружній модуль. Модуль пружності мембрани поверхневої адсорбції важливий у процесі стабілізації міхура.
③ Формування міцел
Розведені рішення поверхнево -активних речовин підкоряються законам, що супроводжуються ідеальними рішеннями. Кількість поверхнево -активної речовини на поверхні розчину збільшується при концентрації розчину, і коли концентрація досягає або перевищує певне значення, кількість адсорбції більше не збільшується, і ці молекули надлишкового ПАР у розчині в розчині або регулярно. І практика, і теорія показують, що вони формують асоціації в рішеннях, і ці асоціації називаються міцелами.
Критична концентрація міцел (CMC): Мінімальна концентрація, при якій поверхнево -активні речовини утворюють міцели в розчині, називається критичною концентрацією міцел.
④ Значення CMC загальних ПАР.

HLB - це абревіація гідрофільного ліпофільного балансу, що вказує на гідрофільний та ліпофільний баланс гідрофільних та ліпофільних груп ПАР, тобто значення HLB поверхнево -активної речовини. Велике значення HLB вказує на молекулу з сильною гідрофільністю та слабкою ліпофільністю; І навпаки, сильна ліпофільність та слабка гідрофільність.
① Положення вартості HLB
Значення HLB є відносним значенням, тому, коли значення HLB розробляється як стандарт, значення HLB парафінового воску, яке не має гідрофільних властивостей, визначається 0, тоді як значення HLB додецилсульфату натрію, яке є більш водорозчинним, становить 40. 10 - ліпофільні, тоді як ті, що перевищують 10, гідрофільні. Таким чином, перелом від ліпофільного до гідрофільного становить близько 10.
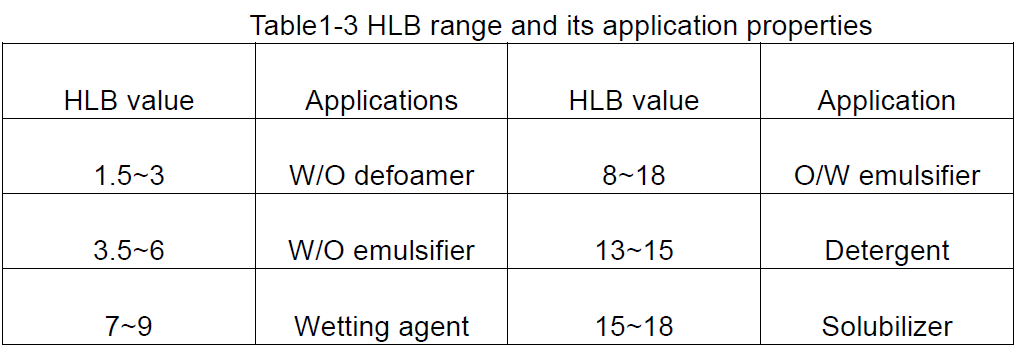
На основі значення HLB поверхнево-активних речовин можна отримати загальне уявлення про їх можливе використання, як показано в таблиці 1-3.

Дві взаємно нерозчинні рідини, одна диспергована в іншій як частинки (краплі або рідкі кристали) утворюють систему, що називається емульсією. Ця система є термодинамічно нестабільною через збільшення прикордонної області двох рідин при утворенні емульсії. Для того, щоб зробити емульсію стабільною, необхідно додати третій компонент - емульгатор для зменшення міжфазної енергії системи. Емульгатор належить до ПАР, його основна функція - відігравати роль емульсії. Фаза емульсії, яка існує як краплі, називається дисперсною фазою (або внутрішньою фазою, переривчастою фазою), а інша фаза, яка пов'язана між собою, називається дисперсійною середовищем (або зовнішньою фазою, безперервною фазою).
① емульгатори та емульсії
Поширені емульсії, одна фаза-це водний або водний розчин, інша фаза-це органічні речовини, не зловмисні з водою, наприклад, жиром, воском тощо (вода/олія). Також може бути сформована складна вода-олія у воді з/о/в тип та масляно-вода-в олії O/W/O.
Емульгатори використовуються для стабілізації емульсій за рахунок зменшення міжфазної напруги та утворення одномолекулярної міжфазної мембрани.
В емульгуванні вимог емульгаторів:
Відповідь: емульгатор повинен мати можливість адсорбуючи або збагатити інтерфейс між двома фазами, щоб зменшити міжфазний натяг;
B: Емульгатор повинен надати частинкам заряд, так що електростатичне відштовхування між частинками або утворює стабільну, сильно в'язку захисну мембрану навколо частинок.
Тому речовина, що використовується як емульгатор, повинна мати амфіфільні групи з метою емульгування, і поверхнево -активні речовини можуть відповідати цій вимозі.
② Методи підготовки емульсій та факторів, що впливають на стабільність емульсій
Існує два способи приготування емульсій: один - використовувати механічний метод для розповсюдження рідини в крихітних частинках в іншій рідині, яка в основному використовується в промисловості для приготування емульсій; Інший - розчиняти рідину в молекулярному стані в іншій рідині, а потім змусити її правильно зібрати, щоб утворити емульсії.
Стабільність емульсії-це здатність до агрегації античастинок, що призводить до поділу фаз. Емульсії - це термодинамічно нестабільні системи з великою вільною енергією. Тому так звана стабільність емульсії-це фактично час, необхідний для того, щоб система досягла рівноваги, тобто час, необхідний для поділу однієї з рідин у системі.
Коли міжфазна мембрана з жирними спиртами, жирними кислотами та жирними амінами та іншими полярними органічними молекулами, міцність мембран значно вища. Це пояснюється тим, що в міжфазному адсорбційному шарі молекул та спиртів, кислот та амінів та інших полярних молекул емульгаторів, щоб утворити «комплекс», так що міцність міжфазної мембрани зростала.
Емульгатори, що складаються з більш ніж двох поверхневих речовин, називаються змішаними емульгаторами. Змішаний емульгатор, адсорбований на інтерфейсі води/масла; Міжмолекулярна дія може утворювати комплекси. Через сильну міжмолекулярну дію міжфазне напруження значно знижується, кількість емульгатора, адсорбованого в інтерфейсі, значно збільшується, утворення щільності міжфазної мембрани збільшується, збільшується міцність.
Заряд рідких намистин суттєво впливає на стабільність емульсії. Стабільні емульсії, чиї рідкі намистини, як правило, заряджаються. Коли використовується іонний емульгатор, іон емульгатора, адсорбований на інтерфейсі, має свою ліпофільну групу, вставлену в масляну фазу, а гідрофільна група знаходиться у водній фазі, тим самим роблячи рідкі намистини зарядженими. Оскільки намистини емульсії з однаковим зарядом, вони відбивають один одного, нелегко агломератувати, щоб підвищити стабільність. Видно, що чим більше іонів емульгату, адсорбованих на намистинах, тим більший заряд, тим більша здатність запобігти намистинам від агломерації, тим стабільнішою емульсійною системою.
В'язкість дисперсійного середовища емульсії має певний вплив на стабільність емульсії. Як правило, чим вище в'язкість дисперсійного середовища, тим вище стабільність емульсії. Це пояснюється тим, що в'язкість дисперсійного середовища велика, що сильно впливає на броунівський рух рідких намистин і уповільнює зіткнення між рідиною намистинами, щоб система залишалася стабільною. Зазвичай полімерні речовини, які можуть бути розчинені в емульсіях, можуть збільшити в'язкість системи та зробити стабільність емульсій вища. Крім того, полімери також можуть утворювати сильну міжфазну мембрану, що робить емульсійну систему більш стійкою.
У деяких випадках додавання суцільного порошку також може зробити емульсію, як правило, стабілізується. Твердий порошок знаходиться у воді, олії або інтерфейсі, залежно від олії, води на змоченій ємності твердого порошку, якщо твердий порошок не повністю вологий водою, а також мокрою олією, залишатиметься на воді та масляному інтерфейсі.
Суцільний порошок не робить емульсією стійкою, оскільки порошок, зібраний на інтерфейсі, посилює міжфазну мембрану, яка схожа на міжфазну адсорбцію молекул емульгату, тому більш тісно твердий порошок матеріал розташований на інтерфейсі, тим стабільніша емульсія.
Поверхнево-активні речовини мають здатність значно збільшити розчинність нерозчинних або злегка водорозчинних органічних речовин після утворення міцел у водному розчині, і розчин прозорий в цей час. Цей ефект міцели називається солюбілізацією. ПАР, яка може виробляти солюбілізацію, називається солюбілізатором, а органічна речовина, яка є солюбілізованою, називається солюбілізованою речовиною.

Піна відіграє важливу роль у процесі прання. Піна - це дисперсійна система, в якій газ розповсюджується в рідину або тверді, з газом як дисперсована фаза та рідина або тверда речовина, як диспергування, перша називається рідкою піною, а другий називається твердою піною, такою як пінопласт, пінопласт, пінопласт тощо.
(1) Формування піни
Під піною ми маємо на увазі тут сукупність повітряних бульбашок, розділених рідкою мембраною. Цей тип міхура завжди швидко піднімається до поверхні рідини через велику різницю щільності між дисперсною фазою (газом) та дисперсійною середовищем (рідиною), поєднаному з низькою в'язкістю рідини.
Процес утворення бульбашки полягає в тому, щоб принести в рідину велику кількість газу, а бульбашки в рідині швидко повертаються на поверхню, утворюючи сукупність бульбашок, розділених невеликою кількістю рідкого газу.
Піна має дві значущі характеристики з точки зору морфології: одна полягає в тому, що бульбашки як дисперсної фази часто мають багатогранну форму, це тому, що на перехресті бульбашок є тенденція до того, що рідка плівка до певної міри стала, коли рідка плівка в певній мірі призводить до бульбашкового розриву; Друга полягає в тому, що чисті рідини не можуть утворювати стабільну піну, рідина, яка може утворювати піну, - це щонайменше два або більше компонентів. Водні розчини ПАР типовий для систем, схильних до генерації піни, і їх здатність генерувати піну також пов'язана з іншими властивостями.
Поверхнево -активні речовини з хорошою піноутворенням називаються піноутворюючими агентами. Хоча пінильний агент має хорошу здатність до піни, але сформована піна може не підтримувати тривалий час, тобто її стабільність не обов'язково хороша. Для підтримки стабільності піни, часто в піноутворюванні для додавання речовин, які можуть підвищити стабільність піни, речовина називається стабілізатором піни, зазвичай використовується стабілізатор, є лаврил -діетаноламіном та оксидом додецил диметиламіну.
(2) Стабільність піни
Піна - це термодинамічно нестабільна система, і кінцева тенденція полягає в тому, що загальна площа поверхні рідини всередині системи зменшується після того, як міхур зламається, а вільна енергія зменшується. Процес дефоміна - це процес, за допомогою якого рідка мембрана, що розділяє газ, стає більш товстим і тоншим, поки він не зламається. Тому ступінь стабільності піни в основному визначається швидкістю розряду рідини та міцністю рідкої плівки. Наступні фактори також впливають на це.
(3) знищення піни
Основним принципом руйнування піни є зміну умов, що виробляють піну, або усунення стабілізуючих факторів піни, таким чином існують як фізичні, так і хімічні методи дефоамування.
Фізичне дефомінг означає зміну умов виробництва піни, зберігаючи хімічний склад розчину піни, такі як зовнішні порушення, зміни температури або тиску та ультразвукову обробку - це всі ефективні фізичні методи для усунення піни.
Метод хімічного дефоамування полягає в тому, щоб додати певні речовини для взаємодії з піноутворюючим агентом для зниження міцності рідкої плівки в піні і, таким чином, зниження стабільності піни для досягнення мети розбещення, такі речовини називаються дефоамерами. Більшість дефоамерів - поверхнево -активні речовини. Тому, згідно з механізмом дефоамінгу, дефоамер повинен мати сильну здатність зменшити поверхневий натяг, легко адсорбується на поверхні, а взаємодія між поверхневими молекулами адсорбції є слабкою, адсорбційні молекули, розташовані в більш розслабленій структурі.
Існують різні типи дефоамер, але в основному всі вони неіонні ПАР. Неіонні поверхнево-активні речовини мають властивості анти-спритності поблизу або вище їх хмарної точки і часто використовуються як дефоамери. Спирти, особливо спирти з розгалуженою структурою, жирними кислотами та ефірами жирних кислот, поліамідами, ефірами фосфатів, силіконовими маслами тощо, також зазвичай використовуються як відмінні дефоамери.
(4) піна і миття
Немає прямого зв’язку між піною та ефективністю прання та кількістю піни не вказує на ефективність промивання. Наприклад, неіонні поверхнево -активні речовини мають набагато менше спінених властивостей, ніж мила, але їх дезактивація набагато краще, ніж мило.
У деяких випадках піна може бути корисною для видалення бруду та бруду. Наприклад, під час промивання посуду в будинку піна миючого засобу підбирає краплі масла та при очищенні килимів піна допомагає забрати пил, порошок та інший твердий бруд. Крім того, піну іноді можна використовувати як вказівку на ефективність миючого засобу. Оскільки жирні олії пригнічують вплив на піну миючого засобу, коли нафти занадто багато і занадто мало миючого засобу, піни не будуть генеруватися або первісна піна зникне. Піні також іноді можна використовувати як індикатор чистоти полоскання, оскільки кількість піни в розчині полоскання має тенденцію до зменшення миючого засобу, тому кількість піни може бути використана для оцінки ступеня полоскання.
У широкому розумінні миття - це процес видалення небажаних компонентів з об'єкта, який слід промивати та досягти певної мети. Миття у звичайному сенсі відноситься до процесу видалення бруду з поверхні носія. При промиваннях взаємодія між брудом і носієм ослаблена або усувається дією деяких хімічних речовин (наприклад, миючий засіб тощо), так що комбінація бруду та носія змінюється на поєднання бруду та миючого засобу, і нарешті бруд відокремлюється від носія. Оскільки об'єкти, які слід промивати, і бруд, який слід видалити, різноманітні, миття - це дуже складний процес, і основний процес промивання може бути виражений у наступних простих відносинах.
Керрі ·· бруд + миючий засіб = носій + бруд · миючий засіб
Процес промивання зазвичай можна розділити на два етапи: по -перше, під дією миючого засобу бруд відокремлюється від його носія; По -друге, відокремлений бруд розповсюджується і призупиняється в середовищі. Процес промивання є оборотним процесом, а бруд розповсюджена та підвішений у середовищі також може бути повторно наданий від середовища до об'єкта, що промиається. Тому хороший миючий засіб повинен мати здатність розсіювати та призупиняти бруд та запобігти переробленню бруду, крім здатності видаляти бруд з носія.
(1) Типи бруду
Навіть для одного і того ж елемента тип, композиція та кількість бруду можуть змінюватись залежно від середовища, в якому він використовується. Бруд нафти нафти - це в основному деякі тваринні та рослинні олії та мінеральні олії (наприклад, сире олія, мазум, вугільний дьогтям тощо), твердий бруд - це в основному сажа, зола, іржа, чорний вуглець тощо. З точки зору бруду, бруд з людського тіла є бруд, такі як піт, сала, кров тощо; бруд з їжі, такі як плями з фруктами, кулінарні плями, плями приправи, крохмаль тощо; бруд від косметики, наприклад, помада, лак для нігтів тощо; бруд з атмосфери, наприклад, сажа, пил, грязь тощо; Інші, такі як чорнило, чай, покриття тощо. Він випускається в різних типах.
Різні типи бруду зазвичай можна розділити на три основні категорії: твердий бруд, рідкий бруд та спеціальний бруд.
① Суцільний бруд
Поширений твердий бруд включає частинки золи, грязі, землі, іржі та вуглецю. Більшість цих частинок мають електричний заряд на своїй поверхні, більшість з них негативно заряджені і можуть легко адсорбуватись на предметах волокна. Твердий бруд, як правило, важко розчиняти у воді, але його можна розповсюджувати та суспендувати за допомогою миючих розчинів. Тверда бруд з меншими масовими точками складніше видалити.
② Рідкий бруд
Рідка бруд-здебільшого нафторозчинна, включаючи рослинні та тваринні олії, жирні кислоти, жирні спирти, мінеральні олії та їх оксиди. Серед них можуть відбуватися рослинні та тваринні олії, жирні кислоти та лужне омивання, тоді як жирні спирти, мінеральні олії не оминуть лугом, але можуть бути розчинними в спиртах, ефірі та вуглеводневих органічних розчинниках та розчині водних миючих засобів. Розчинна нафторозчинна рідина бруд, як правило, має сильну силу з предметами волокна, і більш міцно адсорбується на волокнах.
③ Спеціальний бруд
Спеціальний бруд включає білки, крохмаль, кров, людські виділення, такі як піт, шкірне сок, сеча та фруктовий сік та чайний сік. Більшість цього типу бруду може бути хімічно і сильно адсорбований на предметах волокна. Тому це важко мити.
Різні типи бруду рідко зустрічаються поодинці, але часто змішуються разом і адсорбуються на об'єкт. Бруд іноді можна окислювати, розкладати або розпадати під зовнішніми впливами, створюючи тим самим новий бруд.
(2) Адгезія бруду
Одяг, руки тощо можна забарвити, оскільки існує якась взаємодія між предметом і брудом. Бруд дотримується предметів різними способами, але фізичних та хімічних спайок не більше.
① Адгезія сажі, пилу, грязі, піску та деревного вугілля до одягу - це фізична адгезія. Взагалі кажучи, завдяки цій адгезії бруду та ролі між забарвленим предметом є відносно слабка, видалення бруду також відносно легке. Згідно з різними силами, фізична адгезія бруду може бути розділена на механічну адгезію та електростатичну адгезію.
A: Механічна адгезія
Цей тип адгезії в основному відноситься до адгезії якоїсь твердої бруду (наприклад, пил, грязь та пісок). Механічна адгезія є однією з слабших форм адгезії бруду і може бути видалена майже чисто механічними засобами, але коли бруд невеликий (<0,1um), її складніше видалити.
B: Електростатична адгезія
Електростатична адгезія в основному проявляється в дії заряджених частинок бруду на протилежно заряджених предметах. Більшість волокнистих об'єктів негативно заряджаються у воді і легко можуть дотримуватися певного позитивно зарядженого бруду, наприклад типів вапна. Деякі бруд, хоча негативно заряджені, такі як частинки вуглецю у водних розчинах, можуть дотримуватися волокон через іонні мости (іони між множинними протилежно зарядженими предметами, діючи разом з ними мостовим способом), утворених позитивними іонами у воді (наприклад, Ca2+ , mg2+ тощо).
Електростатична дія сильніша, ніж проста механічна дія, що ускладнює видалення бруду.
② Хімічна адгезія
Хімічна адгезія відноситься до явища бруду, що діє на предмет через хімічні або водневі зв’язки. Наприклад, полярний твердий бруд, білок, іржа та інша адгезія на предметах волокон, волокна містять карбоксильні, гідроксильні, амідні та інші групи, ці групи та жирні кислоти жирного бруду, жирні спирти легко утворювати водневі зв’язки. Хімічні сили, як правило, сильні, і бруд більш міцно пов'язаний з об'єктом. Цей тип бруду важко видалити звичайними методами і вимагає спеціальних методів вирішення з ним.
Ступінь адгезії бруду пов'язана з природою самого бруду та природою об'єкта, до якого він дотримується. Як правило, частинки легко дотримуються фіброзних предметів. Чим менша текстура твердого бруду, тим сильніша адгезія. Полярний бруд на гідрофільних предметах, таких як бавовна та скло, прилягають сильніше, ніж неполярний бруд. Неполярний бруд дотримується сильніше, ніж полярний бруд, такі як полярні жири, пил і глина, і його менш простий у видаленні та очищення.
(3) Механізм видалення бруду
Мета промивання - видалити бруд. У середовищі певної температури (переважно води). Використовуючи різні фізичні та хімічні ефекти миючого засобу для послаблення або усунення ефекту від бруду та промитого предметів, під дією певних механічних сил (таких як втирання рук, агітація пральної машини, вплив води), так що бруд та промивані предмети з мети дезактивації.
① Механізм видалення рідини
: Змочування
Рідке забруднення в основному нафта на масляній основі. Масляні плями з мокрими найбільш волокнистими предметами і розкладаються більш -менш, як масляна плівка на поверхні волокнистого матеріалу. Перший крок у дії промивання - це змочування поверхні промитою рідиною. Для ілюстрації поверхню волокна можна вважати гладкою твердою поверхнею.
B: Затінок нафти - механізм завивки
Другий крок у дії промивання - це видалення нафти та жиру, видалення рідкого бруду досягається різновидом згортання. Рідкий бруд спочатку існував на поверхні у вигляді розповсюдженої масляної плівки, а під переважним нав'язливим ефектом промивної рідини на тверду поверхню (тобто поверхня волокна) вона згорнулася в крок за крок за кроком, які були замінені промитою рідиною і з часом покинули поверхню під певними зовнішніми силами.
② Механізм видалення твердого бруду
Видалення рідини бруду в основному через переважне змочування носія бруду за допомогою промивання розчину, тоді як механізм видалення твердого бруду відрізняється, де процес промивання в основному про змочування маси бруду та поверхні її носія за допомогою промивання розчином. Завдяки адсорбції ПАР на твердій бруді та поверхні його носія, взаємодія між брудом і поверхнею зменшується і міцність адгезії бруду на поверхні зменшується, таким чином маса бруду легко видаляється з поверхні носій.
Крім того, адсорбція ПАР, особливо іонних поверхнево -активних речовин, на поверхні твердого бруду та його носія, має потенціал для збільшення поверхневого потенціалу на поверхні твердого бруду та його носія, який є більш сприятливим для видалення бруду. Тверді або загалом волокнисті поверхні зазвичай негативно заряджаються у водних середовищах і, отже, можуть утворювати дифузні подвійні електронні шари на брудних масах або твердих поверхнях. Через відштовхування однорідних зарядів адгезія частинок бруду у воді до твердої поверхні ослаблена. Коли додається аніонна поверхнево -активна речовина, оскільки він може одночасно збільшити негативний поверхневий потенціал частинки бруду та тверду поверхню, відштовхування між ними посилюється, міцність адгезії частинки зменшується, а бруд легше видалити.
Неіонні поверхнево-активні речовини адсорбуються на загально заряджених твердих поверхнях, і хоча вони не значно змінюють міжфазний потенціал, адсорбовані неіонні поверхнево-активні речовини, як правило, утворюють певну товщину адсорбованого шару на поверхні, що допомагає запобігти переодягненню бруду.
У випадку катіонних поверхнево -активних речовин їх адсорбція зменшує або усуває негативний поверхневий потенціал бруду та поверхні її носія, що зменшує відштовхування між брудом і поверхнею і тому не сприяє видаленню бруду; Крім того, після адсорбції на твердій поверхні катіонні поверхнево -активні речовини, як правило, перетворюють тверду поверхневу гідрофобну і, отже, не сприяють поверхневому змоченому і тому промиванню.
③ Видалення спеціальних ґрунтів
Білок, крохмаль, людські виділення, фруктовий сік, чайний сік та інший такий бруд важко видалити з нормальними поверхневими речовинами і потребують спеціального лікування.
Плями білка, такі як вершки, яйця, кров, молоко та шкірна екскрета, як правило, згортаються на волокнах і дегенерації і отримують сильнішу адгезію. Білкове забруднення можна видалити за допомогою протеаз. Ферментна протеаза розбиває білки в бруді у водорозчинні амінокислоти або олігопептиди.
Плями крохмалю в основному надходять з продуктів харчування, інші, такі як підливка, клей тощо. Амілаза має каталітичний вплив на гідроліз крохмальних плям, внаслідок чого крохмаль руйнується на цукри.
Ліпаза каталізує розкладання тригліцеридів, які важко видалити звичайними методами, такими як шкірні та їстівні олії, і розбиває їх на розчинний гліцерин та жирні кислоти.
Деякі кольорові плями з фруктових соків, чайних соок, чорнила, помади тощо часто важко очистити навіть після повторного промивання. Ці плями можна видалити окислювально-відновлювальною реакцією з окислювальним або відновлюючим агентом, таким як відбілювач, який руйнує структуру кольорових або кольорових груп, а також погіршує їх у менші водорозчинні компоненти.
(4) Механізм видалення плям сухого очищення
Вищезазначене насправді для води як середовища промивання. Насправді, завдяки різним видам одягу та споруди, деякий одяг, що використовує промивання води, не є зручним або не простим для миття чистого, одягу після промивання та навіть деформації, вицвілення тощо, наприклад: більшість природних волокон поглинають воду і легко набрякли, і сухе і легко зменшуватися, тому після промивання буде деформовано; Промивши вовняні вироби також часто виявляється явищем усадки, деякі вовняні вироби з промиванням води також простіть у стовпах, зміна кольору; Деякі шовки почувають себе гірше після миття і втрачають блиск. Для цього одягу часто використовують метод сухого очищення для знезараження. Так зване сухе очищення, як правило, стосується методу промивання в органічних розчинниках, особливо в неполярних розчинниках.
Сухе очищення - це більш ніжна форма промивання, ніж миття води. Оскільки сухе чистка не потребує великої механічної дії, це не спричиняє пошкодження, зморшок та деформації одягу, тоді як засоби для сухого очищення, на відміну від води, рідко виробляють розширення та скорочення. Поки технологія належним чином обробляється, одяг може бути сухий без спотворення, вицвітання кольору та тривалий термін служби.
Що стосується сухого очищення, то є три широкі типи бруду.
①oil-розчинна брудна брудна бруд включає всі види масла та жиру, яка є рідкою або жирною і може бути розчиняється в сухих очисних розчинниках.
② Воднорозчинна брудна брудна бруд розчинна у водних розчинах, але не у сухих очисних засобах, адсорбується на одязі у водному стані, вода випаровується після осадження зернистих твердих речовин, таких як неорганічні солі, крохмаль, білок тощо.
③oil та вода нерозчинна брудна олія та нерозчинна бруда бруду не є ні розчинними у воді, ні розчинних у сухих очисних розчинниках, таких як вуглець чорного кольору, силікати різних металів та оксидів тощо тощо.
Завдяки різному характеру різних типів бруду, існують різні способи видалення бруду в процесі сухого очищення. Розчинні нафторозчинні ґрунти, такі як тваринні та рослинні олії, мінеральні олії та мастила, легко розчинні в органічних розчинниках і можуть бути легше видаляти при сухому очищенні. Відмінна розчинність розчинників для очищення для масел і мастила по суті походить від сил стінок Ван дер між молекулами.
Для видалення водорозчинної бруду, таких як неорганічні солі, цукри, білки та піт, потрібну кількість води також слід додати до сухого очищення, інакше водорозчинний бруд важко видалити з одягу. Однак воду важко розчинити в агенті з сухим очищенням, тому для збільшення кількості води також потрібно додати ПАР. Наявність води в агенті з химерним очищенням може зробити поверхню бруду та одягу зволоженим, так що легко взаємодіяти з полярними групами ПАР, що сприяє адсорбції ПАР на поверхні. Крім того, коли поверхнево-активні речовини утворюють міцели, водорозчинний бруд та вода можуть бути солюбілізовані в міцели. На додаток до збільшення вмісту води в обчислювальному розчиннику, поверхнево-активні речовини також можуть відігравати роль у запобіганні повторного розгляду бруду для посилення ефекту дезактивації.
Наявність невеликої кількості води необхідна для видалення водорозчинної бруду, але занадто багато води може спричинити спотворення і зморщується в якомусь одязі, тому кількість води в агенті з сухого очищення повинна бути помірною.
Бруд, який не є ні водорозчинним, ані нафторозчинним, тверді частинки, такі як попіл, грязь, земля та чорний вуглець, як правило, прикріплені до одягу електростатичними силами або в поєднанні з олією. У сухому очищенні потік розчинника, удар може зробити електростатичну силу адсорбцією бруду, а засоби для очищення сухого очищення може розчиняти масло, так що комбінація олії та бруду та прикріплення до одягу твердих частинок у сухий очисний агент сухий очисний засіб може бути невелик одяг.
(5) Фактори, що впливають на дії миття
Напряжна адсорбція ПАР на інтерфейсі та зменшення поверхневого (міжфазного) натягу є основними факторами видалення рідини або твердого бруду. Однак процес промивання є складним, а ефект промивання, навіть з тим самим типом миючого засобу, впливає багато інших факторів. Ці фактори включають концентрацію миючого засобу, температуру, природу забруднення, тип волокна та структуру тканини.
① Концентрація ПАР
Міцела ПАР у рішенні відіграють важливу роль у процесі прання. Коли концентрація досягає критичної концентрації міцел (CMC), ефект промивання різко збільшується. Тому концентрація миючого засобу в розчиннику повинна бути вищою, ніж значення CMC, щоб мати хороший ефект промивання. Однак, коли концентрація ПАР вища, ніж значення CMC, поступове збільшення ефекту промивання не є очевидним, і не потрібно занадто збільшувати концентрацію ПАР.
При видаленні олії за допомогою солюбілізації ефект солюбілізації збільшується зі збільшенням концентрації ПАР, навіть коли концентрація вище CMC. У цей час доцільно використовувати миючий засіб місцевим централізованим чином. Наприклад, якщо на манжетах та коміра одягу є багато бруду, під час промивання може бути застосований шар миючого засобу, щоб збільшити розчинний ефект поверхнево -активної речовини на нафту.
② Температура має дуже важливий вплив на дезактивацію. Загалом, підвищення температури полегшує видалення бруду, але іноді занадто висока температура також може спричинити недоліки.
Збільшення температури полегшує дифузію бруду, тверда жира легко емульгуюється при температурі вище його температури плавлення, а волокна збільшують набряк через підвищення температури, всі вони полегшують видалення бруду. Однак для компактних тканин мікрогапі між волокнами зменшуються в міру розширення волокон, що згубно до видалення бруду.
Зміни температури також впливають на розчинність, значення CMC та розмір міцели поверхнево -активних речовин, що впливають на ефект промивання. Розчинність ПАР з довгими вуглецевими ланцюгами низька при низьких температурах, а іноді розчинність навіть нижча, ніж значення CMC, тому температуру промивання слід підвищити належним чином. Вплив температури на значення CMC та розмір міцели відрізняється для іонних та неіонних поверхнево-активних речовин. Для іонних поверхнево -активних речовин підвищення температури, як правило, збільшує значення CMC і знижує розмір міцели, а це означає, що концентрацію ПАР у розчині промивання слід збільшувати. Для неіонних ПАР, підвищення температури призводить до зниження значення CMC та значного збільшення об'єму міцел, тому зрозуміло, що відповідне підвищення температури допоможе неіонному ПАР здійснити його поверхневий активний ефект. Однак температура не повинна перевищувати її хмарної точки.
Коротше кажучи, оптимальна температура промивання залежить від рецептури миючого засобу та промивання об'єкта. Деякі миючі засоби мають хороший миючий засіб при кімнатній температурі, а інші мають значно різну настрою між холодним та гарячим миттям.
③ Піна
Звичайно заплутати спінювальну потужність з ефектом миття, вважаючи, що миючі засоби з високою спіною живлення мають хороший ефект промивання. Дослідження показали, що прямої залежності між ефектом промивання та кількістю піни немає. Наприклад, промивання миючими засобами з низьким вмістом піни не менш ефективно, ніж промивання високими миючими засобами.
Хоча піна не пов'язана безпосередньо з миттям, відбувається випадки, коли вона допомагає видалити бруд, наприклад, при промиванні посуду вручну. Під час очищення килимів піна також може забрати пил та інші тверді частинки бруду, килимовий бруд припадає на велику частку пилу, тому засоби для чищення килимів повинні мати певну здатність до пінопласту.
Сила для піни також важлива для шампунів, де тонка піна, що виробляється рідиною під час шампунь або купання, залишає волосся змащуваними та зручними.
④ Сорти волокон та фізичні властивості текстилю
На додаток до хімічної структури волокон, що впливає на адгезію та видалення бруду, поява волокон та організація пряжі та тканини впливають на легкість видалення бруду.
Ваги вовняних волокон і вигнуті плоскі стрічки бавовняних волокон частіше накопичують бруд, ніж гладкі волокна. Наприклад, вуглецевий чорний, забарвлений на целюлозних плівках (вікозні плівки) легко усунути, тоді як вуглець, забарвлений на бавовняних тканинах, важко вимити. Інший приклад полягає в тому, що тканини з короткочасним з поліестеру більш схильні до накопичення плям нафти, ніж тканини з довгими клітками, а плями з маслом на тканинах з короткими волокнами також складніше видалити, ніж плями нафти на тканинах довгих клітковини.
Щільно закручені нитки та тісні тканини, завдяки невеликому зазору між волокнами, можуть протистояти інвазії бруду, але те саме також може запобігти промивальній рідині, щоб виключити внутрішню бруд, тому тісні тканини починають протистояти бруду, але після заплямованого промивання також складніше.
⑤ Твердість води
Концентрація Ca2+, Mg2+ та інших іонів металів у воді має великий вплив на ефект промивання, особливо коли аніонні поверхнево -активні речовини стикаються з іонами Са2+ та Mg2+, що утворюють солі кальцію та магнію, які є менш розчинними та зменшать його погіршення. У твердій воді, навіть якщо концентрація ПАР висока, все ще набагато гірша, ніж у дистиляції. Щоб поверхнево-активна речовина мала найкращий ефект промивання, концентрацію іонів Са2+ у воді слід знизити до 1 х 10-6 моль/л (CACO3 до 0,1 мг/л) або менше. Це вимагає додавання різних пом'якшувачів до миючого засобу.
Час посади: 25 лютого-2022 рр.



